
Classificação periódica: o que é, tipos e exercícios!
A maioria das salas de aula costumam ter, entre seus objetos, uma tabela explicando a classificação periódica. É um dos diagramas mais emblemáticos e funcionais dos estudos químicos modernos. Apesar de a vermos por aí corriqueiramente, nem sempre conseguimos decifrar seu funcionamento.
Neste artigo, iremos trazer informações sobre a classificação periódica, contando o que é, quais seus tipos, detalhando-os e, no final, você estará pronto para fazer exercícios. É basicamente tudo o que é preciso dominar para responder com tranquilidade às perguntas propostas desse assunto nos vestibulares.
Na verdade, trata-se de um conteúdo muito amplo, que acaba por esbarrar em muitos dos outros temas da disciplina de Química e até mesmo de Biologia ou Geografia. Sendo assim, é muito útil que o vestibulando tenha uma compreensão sólida sobre a classificação periódica dos elementos. Vamos lá?
O que é classificação periódica?
A Tabela Periódica representa os esforços humanos de desvendar quais são e como funcionam os elementos que compõem a natureza, os seres vivos e nosso mundo como um todo. Para se ter ideia, a primeira classificação periódica oficial foi publicada ainda em 1869, pelo químico russo Dmitri Mendeleev.
De lá para cá, muita coisa mudou sobre a compreensão dos elementos. Entretanto, a classificação proposta por ele estava correta em muitos pontos, servindo até hoje como base para a Tabela Periódica que temos atualmente.
Tipos de classificação
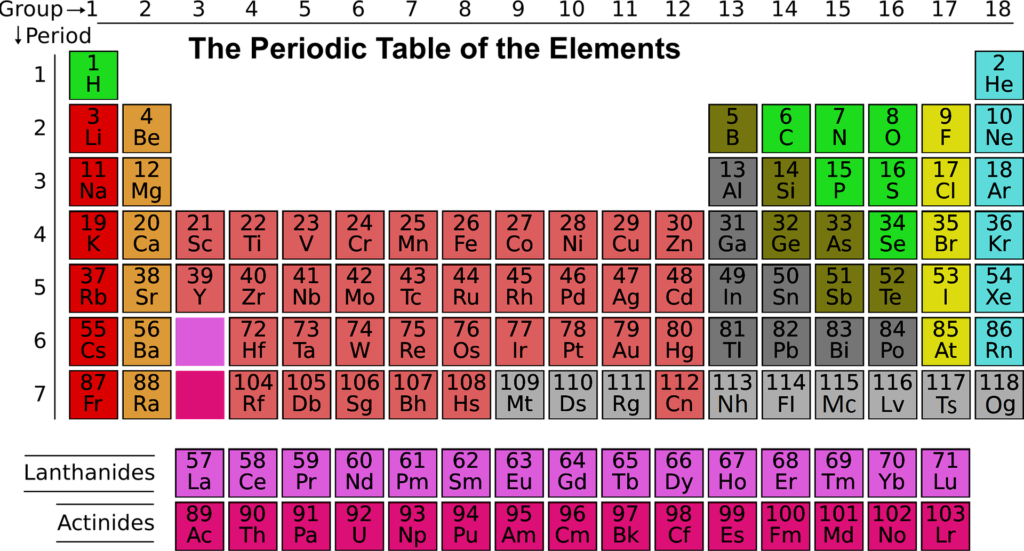
A organização da Tabela Periódica pode ser usada para compreender as relações entre as propriedades dos elementos ali dispostos. Sua classificação principal é a que descreve os grupos e períodos de cada partícula. Além disso, apenas olhando para a Tabela, podemos nos informar sobre o número de átomos e configuração eletrônica de cada elemento.
Grupos
Observado o posicionamento de cada item na Tabela, é possível deduzir o período e a qual grupo ele pertence. Os grupos, ou famílias, são a característica principal e mais importante da classificação periódica. Eles correspondem às colunas do quadro, orientadas no sentido vertical, totalizando uma quantia de 18 famílias nas quais se distribuem todos os elementos.
São conhecidos a partir de sua numeração, mas seis deles recebem também nomes próprios que indicam sua particularidade. O grupo de número 17, por exemplo, são os halogênios. Na última coluna, de número 18, estão contidos os gases nobres.
Períodos
Períodos correspondem às linhas que percorrem o quadro, formadas em sentido horizontal. Pode-se dizer que a classificação por grupos é a que mais diferencia as propriedades dos elementos, mas também podemos observar algumas regras quanto aos períodos.
Eles são ordenados e devem ser lidos da esquerda para a direita. Quanto mais à direita em um período, maior será a chance de que o item seja um metal, ao passo que os localizados mais à esquerda são, geralmente, os não-metálicos.
Gases nobres
Como mencionamos antes, o último grupo da Tabela Periódica recebe o título de gases nobres. Você saberia dizer o que significa esse adjetivo? Receber essa classificação implica algumas características que nos fazem entender o motivo de terem recebido um espaço diferente na tabela. Os gases nobres são conhecidos por:
- serem normalmente encontrados em estado bruto na natureza, de maneira isolada;
- sua forma física mais comum ser a gasosa à temperatura ambiente;
- não formarem ligações facilmente com outros elementos, por isso são popularmente aprendidos como aqueles que “não se misturam” com os outros
Metais
Outra característica importante extraída da classificação periódica diz respeito à propriedade metálica de um elemento. Os metais compõem a grande maioria dos elementos conhecidos pela ciência, ocupando pelo menos dois terços da Tabela e um total de 87 elementos. Suas características são:
- forma física predominantemente sólida, com exceção do mercúrio (Hg), que normalmente encontra-se em estado líquido;
- capacidade de condução de eletricidade e calor;
- maleabilidade, ou seja, capacidade de o elemento químico ser moldado em diferentes estados;
- ductilidade, propriedade que torna os metais fáceis de serem transformados em cabos ou fios condutores de energia.
Ametais e não-metais
O restante da tabela química que não faz parte do grupo dos metais são os ametais ou não-metais. Proporcionalmente, são bem menos diversos do que os anteriores, resumindo-se a 11 elementos.
Quanto à sua localização no quadro periódico, são os que se encontram no canto superior direito, normalmente destacadas com uma coloração diferente do grande grupo dos metais. Suas características são opostas às dos elementos com propriedades metálicas, por isso recebem esse título. Pode-se dizer sobre eles:
- são incapazes de conduzir eletricidade ou calor;
- por conta disso, têm um valor importante como isolantes térmicos e elétricos;
- são difíceis de serem moldados, fragmentam-se com facilidade.
Como exemplos desse grupo, podemos citar: oxigênio (O), carbono (C), enxofre (S) e fósforo (P).
Configuração eletrônica
Por fim, outra característica descrita por meio da classificação periódica é a configuração eletrônica dos elementos. Ela diz respeito à distribuição dos elétrons em um determinado átomo de acordo com seus níveis de energia.
A partir apenas dessa informação, é possível deduzir tanto o grupo quanto o período de um dado elemento. Para isso, usamos o diagrama de energia (ou diagrama de Pauling), que pode ser sobreposto na Tabela Periódica e estabelece a quantidade de elétrons presentes nos níveis de cada átomo.
Exercícios de classificação periódica
Agora que você sabe como funciona a classificação periódica dos elementos, que tal testar os conhecimentos recém-aprendidos com esse par de questões sobre o tema? Os exercícios já foram resolvidos por nós, mas daremos as respostas apenas no final do texto para que você possa tentar por si mesmo. Aqui vão eles:
1. (Stoodi) Ao observarmos a Tabela Periódica, identificamos linhas e colunas. Essas linhas e colunas representam, respectivamente:
a. Famílias ou Grupos e Períodos.
b. Períodos e Famílias ou Grupos.
c. Reatividade e Periodicidade.
d. Períodos e Atomicidade.
e.) Grupos e Reatividade
2. (Stoodi) Cerca de 75% dos elementos presentes na Tabela Periódica são metais. Identifique, entre as alternativas, aquela que apresenta as características dos metais.
a. São todos, sem exceção, sólidos nas condições ambientes e conduzem calor e corrente elétrica.
b. Além de dúcteis e maleáveis e bons condutores de corrente elétrica e calor, os metais são sólidos sem exceção.
c. São sólidos nas condições ambientes (exceto o mercúrio – Hg), são dúcteis e maleáveis, apresentam brilho metálico e são bons condutores de calor e corrente elétrica.
d. Não são bons condutores de calor, mas conduzem facilmente corrente elétrica, além de serem dúcteis e maleáveis.
e. Não conduzem bem corrente elétrica e são facilmente moldáveis em lâminas e fios.
O tema da classificação periódica pode ser muito mais simples do que parece, como você pôde ver. O mais importante é atentar aos conceitos fundamentais de classificação: grupos, períodos, propriedades metálicas etc. A partir disso, você tem uma base de estudo que permitirá conhecer os outros assuntos da Química com muito mais desenvoltura!
Queremos que conheça o Plano de Estudos! Basta acessar e criar sua própria rotina de estudo e acesse informações sobre as últimas provas do Enem!
Resposta das questões
1 – b; 2 – c.